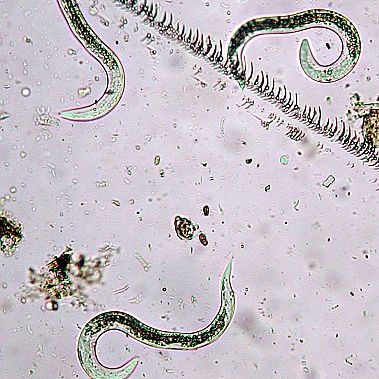
Diagnostik und Monitoring bei Rindern
Diagnostik
Mit einer Kotuntersuchung können Sie mittels eines kombinierten Testverfahrens (Flotation, Sedimentation und Trichterauswanderverfahren nach Baermann-Wetzel) die wichtigsten Wurmarten finden. Da Leberegel nicht gleichmäßig ausgeschieden werden, sind Kotproben entweder zu wiederholen oder der Parasitennachweis geschieht über Schlachthofbefunde, Milch oder Blut.
Untersuchungen auf Parasiten können nicht nur bei Jungrindern sinnvoll sein, sondern beispielsweise auch in der Einzeltierdiagnostik bei Abmagerung, Durchfall oder bei schlechten Leistungen.
Weitere Informationen zu den Nachweismethoden für die einzelnen Wurmarten finden Sie im Folgenden/ unter den jeweiligen Wurmarten (was ist besser?) sowie in der Tabelle Diagnostikverfahren).
Monitoring
Zum Monitoring gehört in allererster Linie die tägliche Tierkontrolle: Fallen Tiere auf? Sehen Sie Abgeschlagenheit (Schlappheit), Durchfall, struppiges Haarkleid, o.ä.? Ist die Körperkondition der Tiere in Ordnung oder sind einige zu dünn? Bei Auffälligkeiten muss genauer untersucht werden.
Für das Monitoring der Belastung der Jungrinder mit MDW können Kotproben (quantitative Verfahren) genutzt werden. Sie sind jedoch mit Vorsicht zu interpretieren. Für Behandlungsentscheidungen sind klinische und Leistungsdaten sowie die Weidehistorie einzubeziehen. Für die Beurteilung der Belastung und des Managements können Blut- oder Milchuntersuchungen auf Ostertagia Anitkörper nach der Weidesaison hilfreich sein.



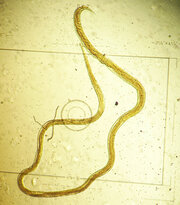
Diagnostik der verschiedenen Wurmarten
Magen-Darm-Würmer
Quantitative Kotuntersuchung (Eizahlbestimmung, FEC, EpG)
Kotuntersuchungen auf Magen-Darm-Würmer (Magen-Darm-Strongyliden) sind wertvoll für das Monitoring der Parasitenbelastung, insbesondere bei erstsömmrigen Jungrindern und für die Wirksamkeitskontrolle nach einer Entwurmung. Diese sollten aber richtig durchgeführt und die Ergebnisse nicht isoliert interpretiert werden.
1. Grundsätzliches zur Probenahme
Alter, Rasse und Produktionsrichtung beeinflussen die Ergebnisse, sowie die beteiligten Wurmarten. Außerdem können die variablen Wetterbedingungen am selben Ort dazu führen, dass die Belastung der Weiden mit Parasitenlarven von Jahr zu Jahr stark variiert. Und der Zeitpunkt ist entscheidend: Im Laufe der Saison nimmt normalerweise die Belastung mit Parasitenlarven auf einer Weide, und damit das Risiko der nicht-immunen Rinder, zu. Am Ende ihrer ersten Weidesaison werden die meisten Jungrinder eine Immunität entwickelt haben und weniger Eier ausscheiden. Die EpG spiegelt ab diesem Zeitpunkt nicht mehr die tatsächliche Wurmbelastung im Tier wider, und andere Messungen (z. B. Gewichtszunahme) können helfen, negative Auswirkungen des Parasitismus bei Jungrindern zu erkennen. Kommen die Tiere erst spät in der Saison auf die Weide, kann auch in der zweiten Saison eine Untersuchung empfehlenswert sein.
2. Wann ist die Eizahlbestimmung sinnvoll?
- Abklärung von Durchfall, Kümmern, Leistungseinbußen
- Wirksamkeitskontrolle von Entwurmungen (Link zur Erklärung Eizahlreduktionstest, FECRT (muss für Rinder überarbeitet werden)
- Kontrolle neu zugekaufter Tiere (Link zur Erklärung Quarantäne(muss für Rinder überarbeitet werden)
- Abschätzung des Infektionsdrucks zu Beginn der Weidesaison (6-8 Wochen nach dem Weideaustrieb bei erstsömmrigen Jungrindern)
- mit Einschränkungen und nur im Zusammenhang mit anderen Kriterien (Klinik, Leistung): für Behandlungsentscheidungen
Für Einzelfälle oder Wirksamkeitstests sind Einzelproben sinnvoll. Beim Eizahlreduktionstest werden die individuellen EpG-Werte vor und 14 Tage nach der Behandlung verglichen. Für das Gruppenmonitoring sind Sammelproben eine kostengünstige Alternative. Es sollten mindestens 10 Tiere bzw. 10 % der Gruppe beprobt werden. Diese Tiere sollten zu einer Altersgruppe (z. B. Kälber, Färsen, Kühe) gehören und unter gleichen Weide- und Managementbedingungen stehen. Vorsicht mit Kotproben von Tieren mit Durchfall, da die Eiausscheidung durch die beschleunigte Darmpassage verfälscht ist. Am besten separat sammeln.
Bei Kotuntersuchungen auf MDS sollte eine quantitative Methode gewählt werden, wie McMaster oder Mini-FLOTAC. Letzteres Verfahren ist aufgrund der hohen Sensitivität für einen Eizahlreduktionstest vorteilhaft. Studien zeigen, dass Sammelproben von etwa zehn Tieren die mittlere Eiausscheidung der Gruppe gut widerspiegeln (Rinaldi et.al., 2019), wenn von jedem Tier die gleiche Menge (z. B. 5 g Kot) in die Probe eingeht.
3. Interpretation der Ergebnisse
Die Eizahl (FEC, wird angegeben in EpG (Eier pro Gramm Kot)) muss vorsichtig interpretiert werden. Es besteht, abhängig von den beteiligten Wurmarten, kein sicherer Zusammenhang zwischen Eiausscheidung und tatsächlicher Wurmbürde. Ausnahme: Jungtiere zu Beginn der Weidesaison. FEC eignet sich gut zur Einschätzung der Weidekontamination. Hierfür wird eine Beprobung 8 Wochen nach Weideauftrieb empfohlen. Bei EpG >200 ist eine Behandlung wahrscheinlich von Vorteil.
Im Herbst können die EpG-Werte der Jungrinder sinken, während klinische Wurminfektionen mit Durchfall oder Abmagerung auftreten. Ursache ist das Zusammenspiel zwischen Wurmbiologie und individueller Immunität, wodurch Eizahl und tatsächliche Wurmbelastung voneinander abweichen können.
Eizahl-Ergebnisse sollten nie isoliert bewertet werden. In die Interpretation sind Alter, Zeitpunkt in der Saison, Weidehistorie, klinischer Zustand/ Leistung und weitere Daten einzubeziehen. Nur im Gesamtkontext lassen sich fundierte Behandlungs- und Managemententscheidungen treffen.
Ergänzende Diagnostik
ELISA (Ostertagia)
Der ELISA-Nachweis basiert auf Antikörpern gegen Ostertagia. Besonders die Tankmilch-ELISA ist eine praktikable und kostengünstige Methode zur Herdenüberwachung im Milchviehbestand Die AK-Bestimmung im Blut kann für die Einschätzung der Belastung der Jungrinder genutzt werden. Die Antikörperkonzentration wird als Optical Density Ratio (ODR) angegeben. Höhere ODR-Werte stehen in Zusammenhang mit geringerer Milchleistung. Werte > 0,5–0,8 (je nach Region) weisen auf ein erhöhtes Risiko produktionsrelevanter Verluste hin.
Die AK-Bestimmungen dienen vor allem der retrospektiven Betrachtung des Parasitenmanagements der vergangenen Weidesaison. Zusammen mit Weidehistorie, Leistungsparametern und anderen Managementinformationen können Schlussfolgerungen für sinnvolle Anpassungen im Folgejahr gezogen werden.
Plasma-Pepsinogen (v. a. Jungtiere)
Die Pepsinogen-Konzentration im Blut spiegelt Schädigungen des Labmagens durch O. ostertagi wider. Besonders bei Kälbern in der ersten Weidesaison korrelieren hohe Werte mit parasitärer Gastroenteritis. Diese Untersuchung wird jedoch derzeit von keinen Laboren angeboten. Nützlich zur Bewertung der Weidestrategie und Planung für das Folgejahr.
Lungenwürmer
Die Diagnose des Lungenwurmbefalls basiert hauptsächlich auf den charakteristischen klinischen Symptomen, die die Tiere auf der Weide zeigen. Wenn Rinder auf der Weide husten, ist meist eine parasitäre Bronchitis die Ursache.
Da die Lungenwurm-Larven selten auf der Weide überwintern, sondern in älteren Rindern oder Kühen, können sich Jungtiere erst dann infizieren, wenn sie auf einer Weide grasen, auf der zuvor solche Larven-Ausscheider waren. Auch dies ist ein diagnostischer Hinweis. Ein weiterer Hinweis ist der Zeitpunkt der Erkrankung. Die meisten Ausbrüche parasitärer Bronchitis treten in der zweiten Hälfte der Weidesaison, also ab Anfang August auf.
Die Diagnose einer Infektion kann durch Kotuntersuchungen bestätigt werden. Nach Anzüchtung aus frischem Kot können die ersten Larven der Lungenwürmer im Labor nachgewiesen werden. Allerdings können Jungrinder schon die Symptome einer Lungenwurmerkrankung zeigen, bevor die ersten Larven im Kot erscheinen.
Leberegel
Auf Herdenebene gibt die Beanstandung von Lebern bei Schlachttieren einen Hinweis, weiter kann Tankmilch auf Antikörper untersucht werden. Die Bestätigung der Verdachtsdiagnose mittels Labordiagnostik ist eine zwingende Voraussetzung für die Behandlung und Bekämpfung des Leberegelbefalls. Obwohl die bovine Fasciolose regional gehäuft vorkommen kann, liegen meist individuelle epidemiologische Situationen auf Betriebsebene vor. Deshalb wird empfohlen, eine an die Betriebssituation angepasste Bekämpfung durchzuführen:
1. In einem bisher noch nicht behandelten Betrieb muss als erster Schritt die betroffene Tiergruppe identifiziert werden: Labordiagnostik sollte bei mindestens 5 Jungtieren (vor der ersten Abkalbung) und bei 5 Milchkühen durchgeführt werden. Bei den Milchkühen sollten vorzugweise die ältesten Tiere untersucht werden, die schon möglichst lange im Betrieb sind. Damit soll unterschieden werden, ob sich Infektionsquellen möglicherweise nur auf Jungtierweiden oder (auch) auf Milchkuhweiden befinden.
2. Im zweiten Schritt müssen Weiden auf potentielle Schneckenlebensräume abgesucht werden und in folgende Gruppen eingeteilt werden:
a) Schneckenlebensräume befinden sich nur auf Jungtierweiden oder auf Weiden für trockenstehende Kühe. Weiden für laktierende Kühe sind nicht betroffen.
b) Schneckenhabitate befinden sich auf allen Weiden für laktierende Kühe.
c) Schneckenhabitate befinden sich auf einzelnen Weiden für laktierende Kühe.
d) Schneckenhabitate befinden sich auf Mähwiesen.
Der Befall mit dem großen Leberegel gilt in einer Herde als nachgewiesen, wenn mindestens ein Tier bei einer labordiagnostischen Untersuchung positiv getestet wurde und mindestens ein Schneckenlebensraum auf den Grünflächen gefunden werden konnte.
Pansenegel
Die Diagnose wird durch den Einachweis im Kot mittels Sedimentationsverfahren gestellt.